Kapittelet omhandler følgende emner:
Hva er gassovermetning?
Hva er løst gass?
Hvordan oppstår gassovermetning?
Måling av TPG
Hvordan unngå gassovermetning?
Passive luftere
Aktive luftere (degassere)
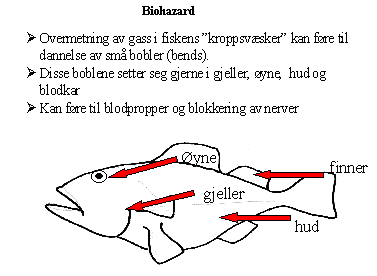
InnledningGassblæresjuke er en tilstand som kan oppstå når vannet som fisken oppholder seg i, er overmettet med gass. Gassovermetning er et fenomen der mer gass enn det vannets løseevne tilsier er tilstede. Dette kan føre til dannelse av små gassbobler både inni og utenpå fisken. I human dykkermedisin er dette fenomenet beskrevet som "dykkersyke" eller "bends". Siden det alltid er nitrogengass som skaper problemer for dykkere, har begrepet "nitrogenovermetning" også festet seg i akvakultursammenheng. Dette har det vist seg ikke nødvendigvis er tilfellet for fisk. Det er totalgassmetningen heller enn nitrogenmetningen som er avgjørende for om det skal kunne dannes bobler eller ikke. Selv om det ikke finnes noe særlig litteratur om grense- eller toleranseverdier for gassovermetning, er indikasjonene at en totalmetning på mer enn 102% gir fisken problemer. Disse grensene vil sannsynligvis være forskjellige fra art til art, men før sikker kunnskap er etablert bør man sørge for at vannet aldri har mer enn 100% totalgassmetning
Dannelse av gassbobler i nervevev og tynne blodkapillærer vil kunne forårsake blokkering av nerveimpulser og blodpropper, med påfølgende alvorlige konsekvenser.
Hva er gassovermetning?
- En tilstand der vannet inneholder mer løst gass pr. volum en løseligheten tilsier.
- Metningsgrad av de ulike gassene er uavhengig av hverandre slik at Nitrogen kan være overmettet mens oksygen er undermettet.
- Men,... Det er totalgasstrykket som bestemmer om det kan oppstå gassbobler. Totalgasstrykket er summen av alle deltrykkene.
Mengden av noen gasser kan måles direkte i vann v.h.a. elektroder, så som Oksygen og ammoniakk. Nitrogen derimot kan ikke måles direkte, men bestemmes indirekte utfra målinger av totalgass (TGP) og oksygen, samt temperatur og barometertrykk (Det er faktisk mulig å måle nitrogengass i vann v.h.a. gasskromatografi, men dette er en omstendelig prosess som ikke brukes i praktiske sammenhenger).
Hva er løst gass?
Gasser kan løse seg i vann, og vil da fortsatt ha formen som et gassmolekyl. Vannlevende dyr er avhengige av løst oksygengass, på samme måte som luftåndere trekker oksygen ut fra lufta. Alle aktuelle gasser har en viss løselighet i vann (a ), som man kan finne empirisk og oversette i en tabell. Løseligheten til en gass i vann er også avhengig av temperatur og salinitet. De gassene man finner i vann kan stamme fra innløsning fra overflaten, eller fra gassproduksjon i vannet, for eksempel av alger.
Når man kjenner Løseligheten kan man finne volumet av løst gass v.h.a. Henry's lov:
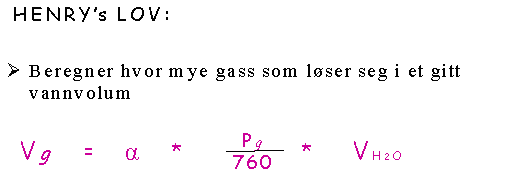
I Henry's lov er Vg volumet av innløst gass, a er løselighetskoeffisienten, Pg er deltrykket til gassen i luften over væsken og VH2O er volumet av vann som gassen skal løses i.
Dersom vannet inneholder MER av en gass enn det Henry's lov tilsier, er vannet overmettet (med denne gassen).
Det man imidlertid skal være klar over er at det er den totale gassmengden (TGP - Total gas pressure, eller Ptot) i vannet som bestemmer om vannet skal være "overmettet". TPG er summen av alle deltrykkene. Dersom denne summen blir høyere enn barometertrykket, vil bobler kunne oppstå. TPG uttrykkes vanligvis som % av fullmetning. Dette er en forståelig og grei måte å uttrykke relativ gassmetning på, sammenlignet med å uttrykke gassmetning som Ptot - Pbar (Totalgasstrykk i vannet minus barometertrykk)
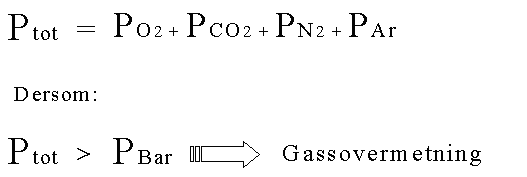
Mengden gass som er løst pr. volum er vanligvis jevnt fordelt i hele vannvolumet fra topp til bunn. Det er imidlertid bare i den helt øverste delen av vannsøylen man normalt opplever en overmetningssituasjon. Dette forklares med det økende hydrostatiske trykket som motvirker tendensen til bobledannelse etter hvert som dybden øker. Dette kalles kompensasjonsdyp:

I akvakultursammenheng er det TPG man derfor skal være oppmerksom på. Er TPG høyere enn 100% er det svært viktig å vite hvilke gasser som bidrar i overmetningen.
Ifølge Henry's lov vil Vg (mengden gass som KAN løses i et vannvolum øke med økende trykk. På 1 meters dyp vil man derfor kunne tolerere en overmetning på 10% uten fare for bobledannelse. (Siden %TPG refereres til barometertrykk vil metningsgrad alltid oppgis "som ved overflaten").
Hvordan oppstår gassovermetning?
I hovedsak to årsaker
1) Innblanding av luft under trykk, f.eks med tørrstilte pumper, eller ved luftbobling i dype kar. Bobling på 1 m dyp vil i teorien kunne gi 10% overmetning (110% TPG). I praksis vil imidlertid dette ikke være tilfelle fordi bobling samtidig lufter av overmetning i de høyere vannlagene.
2) Endring av vannets løselighet. For eksempel ved å øke temperaturen, eller øke saltholdigheten. Et typisk eksempel er at vannet varmes opp etter at det har vært gjennom en tradisjonell kolonnelufter. Som en tommelfingerregel kan man si at for hver grad vannet økes i temperatur, vil gassmetningen øke med 2%. De eksakte verdiene finnes i ulike tabellverk
I tillegg er det mulighet for å få gassovermetning når man blander varmt og kaldt vann. Det er nemlig slik at selv om begge vanntypene er 100% mettet vil det blandede vannet ha en liten overmetning. Som eksempel vil to like volumer av 6 og 12°C vann som begge har 100% TPG, ha 100,4% når de blandes. Dette er små endringer sammenlignet med de tidligere nevnte årsakene, og kan i de fleste tilfeller ses bort fra.
Måling av TPG
Som nevnt er det flere av de "vanlige" gassene som er vanskelige å måle direkte i sjøvann. Den totale metningen (TPG) er imidlertid enkel å måle med det riktige verktøyet. Tensitometeret eller Saturometeret slik vi kjenner det i dag ble først konstruert av Weiss, en Amerikansk biolog for nærmere 50 år siden. Prinsippet er å måle trykket i et nedsenket gassvolum omsluttet av rigide men gasspermeable (slipper gass gjennom) vegger. På denne måten vil gassen i vannet etter en stund komme i likevekt med gassen inne i tensitometeret, og man kan måle Ptot med en vanlig trykkmåler (manometer).
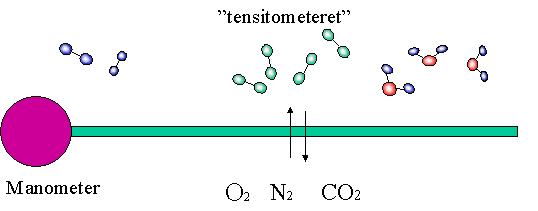
Alle TPG målere arbeider utfra det samme prinsippet. I den senere tid har det imidlertid kommet flere mikroprosessorstyrte modeller på markedet som har innebygde sensorer for oksygen og temperatur, og lufttrykk. Med disse er det mulig å gjøre direkteavlesninger av % metning av både TPG, Nitrogen og oksygen. Skissen viser en gass-del (grønn) som består av en stiv-vegget silikonslange i en lang kveil. I denne slangen foregår utveksling av gass med vann-omgivelsene. Trykket ikke i slangen måles i manometeret (fiolett).
Hvordan unngå gassovermetning
Kun i helt spesielle tilfeller vil man oppleve at vann har overmetning i naturen. Noen eksempler på dette er ved høye forekomster av mikroalger som produserer oksygen, samt i fossefall, der luftbobler blir revet ned på stort dyp. Også i forbindelse med produksjon av vannkraft har det vært eksempler på at vannet nedstrøms har hatt gassovermetning. Man kan imidlertid anta som temmelig sikkert at en marin fisk under naturlige omstendigheter aldri vil oppleve vann med gassovermetning. Det er derfor lite sannsynlig at fisken har en naturlig fluktrespons i kontakt med gassovermetning. I Akvakultursammenheng er gassovermetning dessverre heller regelen enn unntaket. Smoltprodusenter har lenge vært klar over de svært uheldige virkningene av gassovermetning, og tatt konsekvensene av det. I marin yngelproduksjon har man ikke vært like flinke til å etablere rutiner for å unngå overmetning.
Passive luftere
Ulike passive luftere, så som kolonneluftere og INKA-luftere, har lenge vært på markedet. Disse arbeider etter prinsippet om at vann skal "luftes" mot atmosfærisk trykk. Ved å øke vannets overflate mot luft, vil diffusjonsveiene reduseres og avlufting av overmetning vil kunne skje. Diffusjon er imidlertid en langsom prosess, og i beste fall vil man oppnå et vann med 100% TPG. Oppvarming av vannet etter lufteren vil imidlertid føre til gjentatt overmetning.
Aktive luftere (degassere)
Disse kan i teorien arbeide etter to ulike prinsipper:
1) Nitrogenstripping ved gjennombobling med oksygen. Dette er en brukbar metode som gir undermetning av nitrogen, og overmetning av O2 slik at %TPG vil ligge på ca 100. Forhøyet TPG (mer enn 100) kan imidlertid aksepteres så lenge %nitrogenmetning holdes under 100 (helst under 95). Denne metoden krever små investeringer, men blir fort kostbar i drift! Bobling med oksygen representerer også en eksplosjonsfare.
2) Fjerning av gass i vakuum. Denne metoden baserer seg på å redusere Pg delen i Henry's lov. Ved å utsette vann for et undertrykk (ca tilsvarende 1 m vannsøyle) vil løseligheten reduseres med ca 10%. Dette vil føre til en gassovermetning hvor gass fjernes fra vannet. Når vannet "slippes ut" av vakuumet, og trykket blir normalt vil det derimot være undermettet (TPG < BAR). Fordelen med et slikt vann er at det kan tåle en viss oppvarming etter avgassing før overmetning inntrer. En vacuum-degasser vil derfor være en billig forsikring. Selvsagt kan man "toppe" vannet med oksygen etter behov før det tilføres fisketankene.

Både "passive" og "aktive" luftere er handelsvare hos utstyrsleverandører til akvakultur. Her kan man også få råd om dimensjonering.
Revidert: 2005-01-20 11:20:39 |  Vannbehandling
Vannbehandling